
Grundlagen der Gaschromatographie
Dieser Ausarbeitung gibt eine Einführung in die Grundlagen der Gaschromatographie, einer Methode zur Trennung von gasförmigen Proben.
Berechnung der Bindungsenergie von Neon mittels Lennard-Jones-Potential
In dieser kurzen Betrachtung soll die Bindungsenergie von Neon mit Hilfe des Lennard-Jones-Potentials berechnet werden.
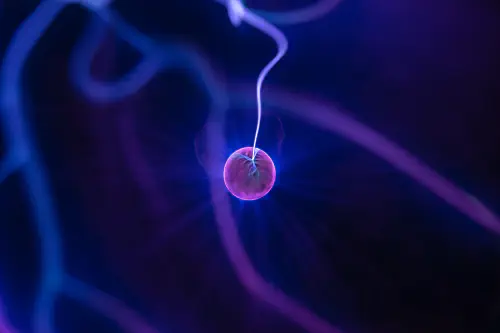
Characterization of a DBD plasma jet for soft ionization
A source for soft ionization of organic molecules is presented in this paper. It is based on an atmospheric pressure dielectric barrier plasma jet, whereby the plasma is ignited inside a glass …

Detection of dissolved metals using a liquid electrode dielectric barrier …
Analysis of dissolved metals in liquid samples using a dielectric barrier discharge with flowing liquid electrode has been studied. Inside a fused-silica capillary the discharge is ignited between the …